Was passiert, wenn Krebs entsteht? Was geschieht dabei mit den zentralen Bausteinen der Zelle, den Proteinen? WissenschafterInnen können sich nun in die kleinsten Strukturen hineinzoomen und deren Aufbau vorhersagen. Ein internationales Team unter der Leitung der University of Washington in Seattle (USA) hat einen neuen Algorithmus entwickelt, der öffentlich verfügbar ist. Uni-Graz-ForscherInnen haben mit Hilfe des Programms RoseTTAfold bisher unbekannte Proteinstrukturen entschlüsselt. Die Türen zur schnelleren Beantwortung biologischer Fragestellungen, wie der Bekämpfung von Krankheiten und der Entwicklung von Medikamenten, stehen nun ganz weit offen.
Das Wissen über Proteine ist essenziell: Die Eiweiß-Verbindungen sind zentrale Bausteine von allen Lebensformen – vom Menschen bis hin zu Bakterien sowie Viren. Darüber hinaus sind sie für wichtige Funktionen wie Stoffwechsel, Transportvorgänge und Signalübertragung in allen Zellen verantwortlich. Eine Veränderung ihrer Struktur und Funktion kann zur Entstehung von Krankheiten führen.
Der Haken: Da sich die Zahl der Proteine auf hunderte Millionen beläuft, ist nur von einem kleinen Bruchteil der genaue Aufbau bekannt. Deren Entschlüsselung mit experimentellen Methoden wäre eine Monsteraufgabe, bestätigt Tea Pavkov-Keller vom Institut für Molekulare Biowissenschaften der Universität Graz. Mit dem neuen Algorithmus ist mit einem Schlag jetzt alles anders. „Woran ich seit Jahren in Form von Experimenten arbeite, lässt sich nun am Computer in wenigen Stunden mit hoher Präzision vorhersagen und führt in Kombination mit experimentellen Daten zur korrekten Struktur“, schwärmt die Forscherin.
„Damit wird die Forschung enorm beschleunigt“, erwartet sich die Strukturbiologin eine rasante Entwicklung in der Medizin und Biotechnologie. Pavkov-Keller: „Zusätzlich können wir vorhersagen, welche Interaktionen zwischen den einzelnen Proteinen passieren. Ebenso erfasst RoseTTAFold jene Eiweiße, die aus mehreren sogenannten Domänen bestehen und sehr oft komplexe Einheiten bilden.“
Die maschinelle Lernfähigkeit, die auf bekannten Sequenzen aufbaut, macht es darüber hinaus möglich, Funktion und Aufgabe der Proteine vorherzusagen. Aufgrund dieser Erkenntnisse lassen sich die Verbindungen gezielt ändern, um zum Beispiel zur Behandlung von Allergien eingesetzt zu werden. Tea Pavkov-Keller spricht von einem Quantensprung: „Die Auswirkungen auf Forschung und technologische Entwicklungen sind derzeit noch gar nicht abschätzbar.“
Die bahnbrechenden Erkenntnisse werden im FWF-geförderten Doktoratsprogramm Doc.funds „Biomolecular Structures and Interactions“ das Forschungstempo immens erhöhen. Das Ausbildungsprogramm wird im Rahmen von BioTechMed-Graz, einer Kooperation der Universität Graz, der Med Uni Graz und der TU Graz, im Herbst starten. Junge ForscherInnen beschäftigen sich mit Biomolekülen, die bei der Signalübertragung und dem Stoffwechsel von Zellen eine wesentliche Rolle spielen.
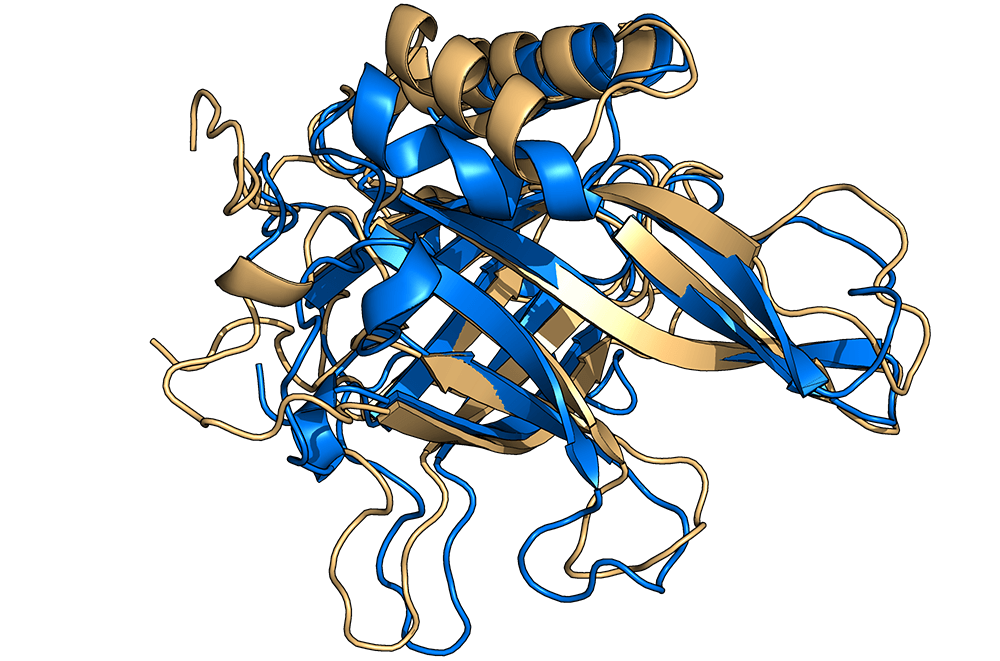
Struktur eines Proteins aus dem Weißfäule-Pilz, berechnet vom Algorithmus RoseTTAFold.



